
抗体医薬品は、副作用の少ない画期的な分子標的薬として、世界で4兆円産業に急成長している。
従来の抗体抗がん剤(第一世代)は、がん細胞を殺すのに、免疫学的なメカニズムを用いる。この方法は、がん細胞の標的分子(下図▼)が沢山あり、抗体が沢山結合することが必須である。副作用は少ないが、効かない患者さんも多い(第一世代抗体薬)。
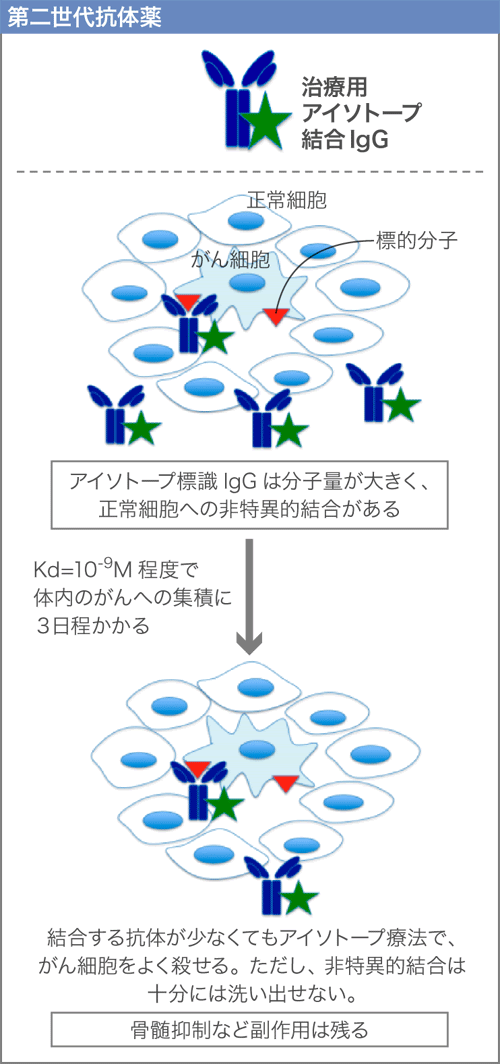
そこで、抗体にアイソトープをつけがん細胞を殺す能力を高める試みが行われている(第二世代)。しかし抗体ががん細胞に結合するまで3日程かかり、非特異的な結合も多いので、放射線の副作用(貧血、白血球減少、血小板減少など)が多くなる(第二世代抗体薬)。
今回、我々は第一、第二世代に加えて、効果は大きく、副作用は少なく、経済負担が軽い第三世代の高機能な分子設計抗体をコンピュータシミュレーションを駆使して開発する(抗体坑がん剤の進化)。
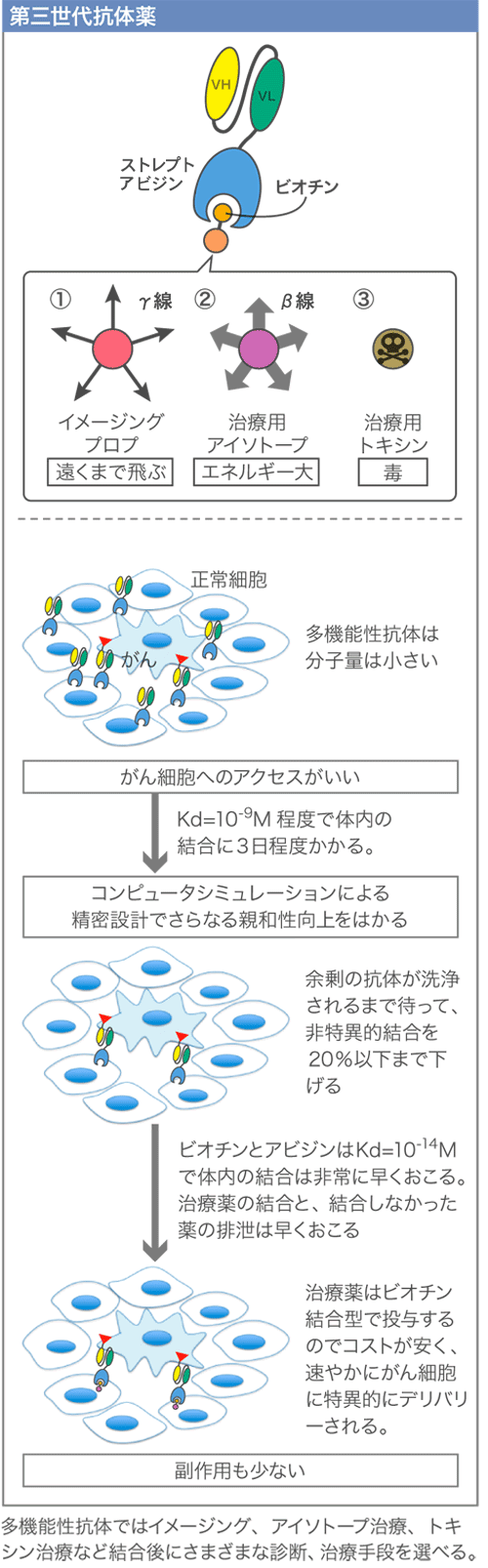
具体的にはがん細胞の認識にかかわるドメインと、治療にかかわるドメインを分離し、がん細胞に結合するscFv改変抗体にはストレプトアビジンを、がん細胞を殺すアイソトープにはビオチンをつける。改変抗体を注射し、がん細胞にだけ結合させ、ビオチンに結合アイソトープを注射し、がん細胞を集中的に治療する(第三世代抗体薬)。
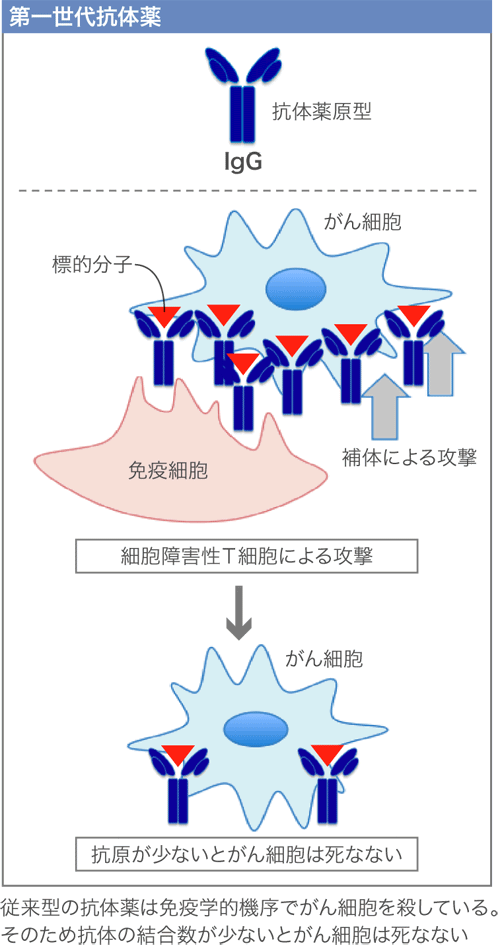
従来の抗体抗がん剤(第一世代)は、がん細胞を殺すのに、免疫学的なメカニズムを用いる。この方法は、がん細胞の標的分子(下図▼)が沢山あり、抗体が沢山結合することが必須である。副作用は少ないが、効かない患者さんも多い(第一世代抗体薬)。
そこで、抗体にアイソトープをつけがん細胞を殺す能力を高める試みが行われている(第二世代)。しかし抗体ががん細胞に結合するまで3日程かかり、非特異的な結合も多いので、放射線の副作用(貧血、白血球減少、血小板減少など)が多くなる(第二世代抗体薬)。
今回、我々は第一、第二世代に加えて、効果は大きく、副作用は少なく、経済負担が軽い第三世代の高機能な分子設計抗体をコンピュータシミュレーションを駆使して開発する(抗体坑がん剤の進化)。
具体的にはがん細胞の認識にかかわるドメインと、治療にかかわるドメインを分離し、がん細胞に結合するscFv改変抗体にはストレプトアビジンを、がん細胞を殺すアイソトープにはビオチンをつける。改変抗体を注射し、がん細胞にだけ結合させ、ビオチンに結合アイソトープを注射し、がん細胞を集中的に治療する(第三世代抗体薬)。



第三世代技術としてGoldenbergらによりプレターゲッティング法が考案された。前もって投与して腫瘍に集積した抗体に対してアビジンービオチン反応を用いて放射性アイソトープを集積させ腫瘍をイメージングまたは治療する方法である。
しかし実験的には著効をあげながらプレターゲッティング治療薬の臨床認可例はまだない。これは、直接的には、scFV-SA化によって抗体のアフィニティーが低下する問題と、ストレプトアビジンの免疫原性が解決されていないためであるが、より大きな問題は、大規模な抗体改変産物を設計して製剤化する困難にある。
抗体改変において、最も多く試みられ有望視されているのは、抗原の決定にかかわる重鎖と軽鎖のFvをリンカーでつないだ最小単位のscFvである。ファージにscFVを発現して、がんを認識するファージを系統的に同定する試みも行われ、多数のがんファージ抗体を取得している。
しかし、scFvをタンパク質医薬品化しようとすると、天然の抗体と比較して、体内動態が異なり、foldingがうまくいかなかったり、発現が低く、凝集しやすく、安定性が悪い、などという問題がある。
東大の津本は、大腸菌でfoldingの巻き戻しによるタンパク発現法を開発している。 診断と治療に役立つヒト型のscFvをマウス抗体遺伝子からいかに迅速に開発できるかに、世界的な競争が繰り広げられている。
しかし実験的には著効をあげながらプレターゲッティング治療薬の臨床認可例はまだない。これは、直接的には、scFV-SA化によって抗体のアフィニティーが低下する問題と、ストレプトアビジンの免疫原性が解決されていないためであるが、より大きな問題は、大規模な抗体改変産物を設計して製剤化する困難にある。
抗体改変において、最も多く試みられ有望視されているのは、抗原の決定にかかわる重鎖と軽鎖のFvをリンカーでつないだ最小単位のscFvである。ファージにscFVを発現して、がんを認識するファージを系統的に同定する試みも行われ、多数のがんファージ抗体を取得している。
しかし、scFvをタンパク質医薬品化しようとすると、天然の抗体と比較して、体内動態が異なり、foldingがうまくいかなかったり、発現が低く、凝集しやすく、安定性が悪い、などという問題がある。
東大の津本は、大腸菌でfoldingの巻き戻しによるタンパク発現法を開発している。 診断と治療に役立つヒト型のscFvをマウス抗体遺伝子からいかに迅速に開発できるかに、世界的な競争が繰り広げられている。

